Negli ultimi anni il legame tra intestino e cervello è uscito dai confini della ricerca di base per diventare uno dei filoni più promettenti nello studio del declino cognitivo. Una recente revisione pubblicata su Nutrition Research ha messo insieme le evidenze disponibili e suggerisce che diversi interventi capaci di modificare il microbiota intestinale – dalla dieta mediterranea ai probiotici, fino ad approcci più sperimentali come il trapianto di microbiota fecale – sembrano condividere alcuni meccanismi biologici associati a un miglioramento delle funzioni cognitive, soprattutto nelle fasi iniziali del deterioramento.
Il punto centrale emerso dalla revisione è che il momento in cui si interviene conta molto. I benefici appaiono infatti più evidenti nelle persone con decadimento cognitivo lieve, o comunque a rischio di demenza, mentre risultano più limitati nei pazienti con malattia di Alzheimer già avanzata. È un dato importante, perché rafforza l’idea che la prevenzione o il trattamento precoce possano avere un ruolo decisivo prima che il danno neurologico diventi troppo esteso.
L’asse intestino – microbiota – cervello
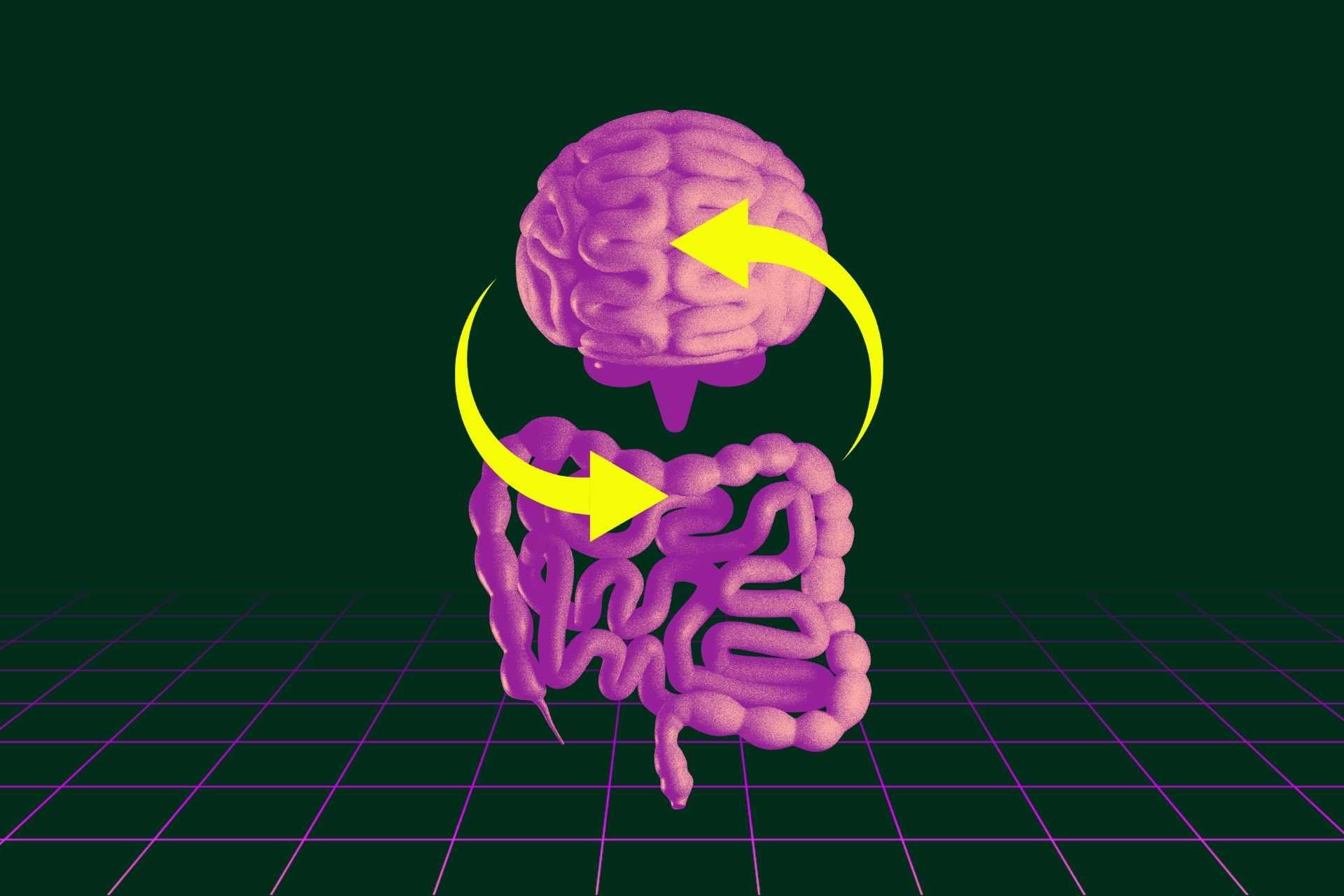
Alla base di questa ipotesi c’è il cosiddetto asse intestino-cervello, un sistema di comunicazione bidirezionale che collega il sistema nervoso centrale e il tratto gastrointestinale attraverso vie nervose, ormonali e immunitarie. Oggi sappiamo che questo dialogo continuo contribuisce a regolare non solo lo sviluppo neurologico e l’umore, ma anche la cognizione. Quando però l’invecchiamento e le abitudini alimentari alterano la composizione del microbiota, può instaurarsi una condizione di disbiosi che, secondo un numero crescente di studi, potrebbe favorire la neurodegenerazione.
Il meccanismo ipotizzato è complesso ma coerente. Una flora intestinale squilibrata può compromettere la barriera epiteliale dell’intestino, permettendo il passaggio nel circolo sanguigno di batteri o di molecole di origine microbica. Questo fenomeno può alimentare uno stato di infiammazione sistemica cronica di basso grado. A sua volta, l’infiammazione sistemica può indebolire la barriera emato-encefalica, rendendo il cervello più esposto a segnali pro-infiammatori. In questo contesto, la neuroinfiammazione può contribuire all’accumulo di proteine anomale come beta-amiloide e tau, caratteristiche della malattia di Alzheimer, e favorire il danno sinaptico e il declino cognitivo.
La revisione ha preso in esame studi condotti su adulti di almeno 45 anni con compromissione cognitiva o con rischio di demenza, valutando diversi tipi di intervento mirati al microbiota. Tra questi figurano probiotici, prebiotici, sinbiotici, integrazione con nutrienti donatori di gruppi metilici, acidi grassi omega-3, trapianto di microbiota fecale e regimi alimentari come la dieta mediterranea o la dieta chetogenica. In totale sono stati inclusi 15 studi, con campioni molto variabili, da appena 5 partecipanti a oltre 1.200, per un totale di 4.275 persone.
Memoria e microbiota intestinale
Pur con limiti metodologici inevitabili, soprattutto negli studi dietetici dove il cieco è difficile da applicare, la qualità complessiva degli studi è risultata nel complesso discreta. I risultati mostrano un’associazione tra la modulazione del microbiota intestinale e il miglioramento di memoria, funzioni esecutive e performance cognitive globali. Ancora una volta, l’effetto più netto è stato osservato nei soggetti con decadimento cognitivo lieve.
Uno degli elementi più interessanti riguarda i possibili meccanismi condivisi da interventi molto diversi tra loro. Molti dei benefici cognitivi osservati sembrano correlati a un aumento della diversità del microbiota e a una maggiore produzione di acidi grassi a catena corta, o SCFA. Queste molecole, prodotte dalla fermentazione delle fibre da parte dei batteri intestinali, sono associate a una riduzione dei marcatori di neuroinfiammazione. Non solo. Gli SCFA sembrano anche contribuire a ridurre lo stress ossidativo e a migliorare la funzione mitocondriale, due aspetti cruciali per la salute neuronale.
In questo quadro la dieta mediterranea e la dieta chetogenica emergono come due approcci di particolare interesse. Entrambe sembrano favorire l’aumento di batteri produttori di SCFA, pur attraverso vie differenti. La dieta mediterranea, ricca di grassi monoinsaturi e composti antiossidanti, promuove un ambiente intestinale con attività antinfiammatoria e antiossidante. La dieta chetogenica, invece, è stata associata a un aumento relativo di specie come Akkermansia muciniphila, note per il loro ruolo nel rafforzare la barriera intestinale e nel promuovere effetti antinfiammatori.
Anche i probiotici mostrano un razionale biologico interessante. Introducendo specifici ceppi batterici, questi interventi potrebbero favorire la produzione di neurotrasmettitori inibitori come il GABA, contribuendo a contrastare gli effetti dannosi di un’eccessiva attività eccitatoria, che è stata collegata sia al decadimento cognitivo lieve sia alla malattia di Alzheimer. Inoltre i probiotici potrebbero sostenere la colonizzazione da parte di microbi capaci di produrre nutrienti neuroprotettivi, migliorare gli scambi metabolici tra ospite e microbiota e ridurre l’infiammazione.
Più esplorativo, ma comunque degno di attenzione, è il tema del trapianto di microbiota fecale. Nella revisione viene citato un piccolo studio preliminare non controllato in cui questo intervento ha indotto modificazioni rapide e stabili del microbiota, associate a un miglioramento dei punteggi cognitivi, a una maggiore diversità batterica e a cambiamenti nell’espressione di geni coinvolti nel metabolismo lipidico. Si tratta però di risultati ancora troppo preliminari per trarre conclusioni solide: servono protocolli standardizzati e dati di lungo periodo per valutarne davvero riproducibilità e rilevanza clinica.
E per quanto riguarda l’Alzheimer?
Un altro aspetto discusso dagli autori riguarda il possibile ruolo del genotipo. L’allele APOE ε4, noto per essere associato a un rischio più elevato di Alzheimer, potrebbe contribuire alla malattia anche attraverso alterazioni del metabolismo lipidico legate alla disbiosi intestinale. Secondo questa ipotesi, i cambiamenti nelle vie lipidiche e nella trasformazione degli acidi biliari da parte del microbiota potrebbero favorire neuroinfiammazione e aumento della permeabilità della barriera emato-encefalica. È un’ipotesi biologicamente plausibile, ma ancora da confermare con studi clinici più ampi e meglio disegnati.
Naturalmente la revisione presenta diversi limiti. Gli studi inclusi erano molto eterogenei per popolazione, tipo di intervento, durata e misure di outcome, tanto che non è stato possibile eseguire una metanalisi. Gli autori hanno quindi optato per una revisione narrativa. Inoltre sono stati considerati solo articoli in lingua inglese, con il rischio di introdurre un bias linguistico. Per questo i risultati vanno interpretati con cautela.
Nonostante queste criticità, il messaggio che emerge è chiaro. Intervenire sul microbiota intestinale potrebbe diventare una delle strategie non farmacologiche più interessanti per sostenere la salute cognitiva, soprattutto nelle fasi iniziali del declino. Dieta, probiotici e altri approcci mirati non vanno considerati scorciatoie né sostituti delle terapie disponibili, ma strumenti potenzialmente complementari a farmaci e modifiche dello stile di vita.
La prospettiva più convincente, almeno per ora, non è quella di una cura miracolosa, ma di un aiuto concreto nel rallentare processi che, una volta avanzati, diventano molto più difficili da modificare. Ed è proprio questo, forse, il dato più rilevante della revisione: quando si parla di cervello e invecchiamento, la finestra di intervento potrebbe aprirsi molto prima di quanto siamo stati abituati a pensare.